科學治療:提高細胞“清潔”能力,或可治療阿爾茨海默病
科學治療:提高細胞“清潔”能力,或可治療阿爾茨海默病
圖片來源:Pixabay
美國阿爾伯特·愛因斯坦醫學院(Albert Einstein College of Medicine)的研究人員設計了一種實驗性藥物,它可以逆轉小鼠阿爾茨海默病(Alzheimer's disease)的主要症狀。該藥物的工作原理是恢複細胞的清潔機製,通過消化和循環的方式來清除不需要的蛋白質。研究已於2021年4月22日在線發表在《細胞》(Cell)雜誌上。
阿爾伯特·愛因斯坦醫學院衰老研究所(the Institute for Aging Research)的聯合主任、發育與分子生物學教授Ana Maria Cuervo是該研究的共同負責人,她對此介紹說:“以往,用小鼠做出的發現並不總能適用於人類,特別是在阿爾茨海默病的研究。但我們此次的研究發現,細胞清潔能力的衰退是阿爾茨海默病的成因之一,這種現象不僅體現在小鼠身上,還發生在人類患者身上。這一發現讓我們備受鼓舞,因為這表明該種藥物或許對人類也同樣有效。”20世紀90年代,Cuervo就發現了這類細胞清潔過程的存在,並將其稱之為“分子伴侶介導的自噬”(chaperone-mediated autophagy,CMA),已經發表了200餘篇有關於其在健康和疾病中的作用的論文。

Ana Maria Cuervo 圖片來源:Albert Einstein College of Medicine
隨著人們年齡的增長,CMA的效率逐漸降低,不必要的蛋白質積聚成有損細胞的不溶性塊狀物的風險也在逐漸增加。事實上,患者大腦中存在有毒蛋白質的聚合物,是阿爾茨海默病和其他所有神經退行性疾病的共有特征。《細胞》上發表的論文揭示了CMA和阿爾茨海默病的動態相互作用:神經元中CMA的缺乏會導致阿爾茨海默病,反之亦然。研究結果表明,加速CMA的藥物可能將為治療神經退行性疾病帶來希望。
建立CMA與阿爾茨海默病之間的聯係
在此項研究中,Cuervo的團隊首先研究了受損的CMA是否會導致阿爾茨海默病。為此,他們對一隻小鼠進行了基因改造,使其大腦內的興奮性神經元缺乏CMA。結果發現,僅一種類型的腦細胞缺失CMA就足以引起短期記憶喪失、行走障礙和其他一些在阿爾茨海默病的齧齒類動物模型中經常發現的問題。此外,在CMA缺失的情況下,蛋白質穩態(proteostasis)將被嚴重破壞,而這是細胞調節其所含蛋白質的能力。通常情況下,可溶性蛋白質會變為不可溶,具有凝結成有毒聚合物的風險。
Cuerve對該現象的逆向懷疑也是正確的:早期的阿爾茨海默症也同樣會損害CMA。她和同事們對一種相當於早期阿爾茨海默病的小鼠模型進行了研究,在這個模型中,小鼠的大腦神經元能產生tau蛋白的缺陷型拷貝。有證據表明,這種tau蛋白的異常拷貝會聚集在一起,形成神經原纖維纏結(neurofibrillary tangles),導致阿爾茨海默病產生。海馬(hippocampus)是對於記憶和學習而言至關重要的大腦區域,研究團隊重點研究了該區域神經元中的CMA活性,結果發現,與對照組的動物相比,患病小鼠神經元中的CMA活性顯著降低。
那處於早期的阿爾茨海默病的人類患者呢?它是否也阻礙了(人類細胞的)CMA?為了找到答案,研究人員對阿爾茨海默病患者死後的大腦神經元進行了單細胞RNA測序,並與一組來自健康個體的對照組數據進行了比較,希望了解CMA在患者腦組織中的活動水平。果然,處於阿爾茨海默病早期階段的患者,其CMA活性受到了一定程度的抑製;在阿爾茨海默症的晚期階段,這種抑製情況更為嚴重。
Cuervo表示:“當人們到了70或80歲時,CMA活動水平通常會比他們年輕時減少約30%。雖然大多數人的大腦可以彌補這種衰退,但如果此時再加上神經退行性疾病,這對大腦神經元的正常蛋白質組成可能是毀滅性的影響。我們的研究表明,CMA功能缺陷與阿爾茨海默病的病理過程協同作用,這將大大加速疾病的發展。”
一種“清潔”神經元的新藥
基於這一令人備受鼓舞的發現,Cuervo和團隊開發了一種新藥,這種藥物顯現出治療阿爾茨海默病的潛力。Cuervo介紹說:“我們知道CMA能夠消化有缺陷的tau蛋白和其他蛋白。但是阿爾茨海默病和其他神經退行性疾病中,大量的缺陷蛋白讓CMA不堪重負、並使其最終癱瘓。而我們的藥物能夠通過提高CMA關鍵成分的水平來重振CMA的效率。”
在CMA中,一種被稱為分子伴侶(chaperones)的蛋白質會與機體細胞中受損或有缺陷的蛋白質結合,並將它們當作“貨物”一般運輸至細胞的溶酶體(lysosomes)。作為一種內部充滿酶的膜結合型細胞器,溶酶體能起到消化和回收廢物的作用。然而,為了能成功地將這些“貨物”送入溶酶體,分子伴侶必須首先將它們“停靠”至稱為LAMP2A的蛋白質受體“船塢”上,而這種受體就長在溶酶體的膜上。溶酶體上的LAMP2A受體越多,CMA活性就可能越高。這款被稱為CA的新藥,就是通過增加LAMP2A受體的數量來發揮作用。
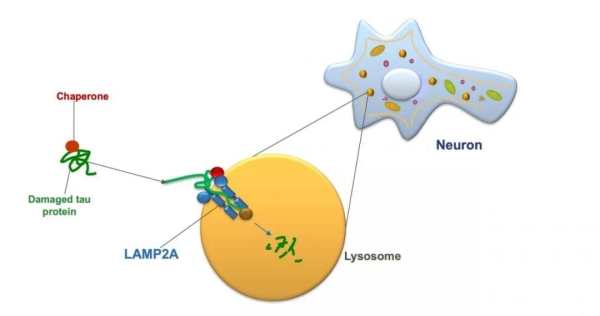
神經元內LAMP2A參與的細胞自噬。圖片來源:Courtesy of Albert Einstein College of Medicine
Cuervo解釋道:“人們一生中所產生的LAMP2A受體數量是相同的。但比起年齡的增加,這些受體的劣化速度更快。所以在老年人體內,將不需要的蛋白質輸送到溶酶體的可用受體往往更少。CA這款藥物能夠將LAMP2A的數量恢複至年輕水平,使CMA能夠有效擺脫tau蛋白和其他蛋白,這樣,它們就不會形成那些有毒的蛋白質團塊了。
同樣在4月,Cuervo博士的團隊在《自然-通訊》(Nature Communications)上報道稱,他們首次從阿爾茨海默病患者的大腦中分離出了溶酶體,並觀察到LAMP2受體數量的減少會導致人類CMA的喪失,就如同在動物模型中所發現的一樣。
研究人員在兩種不同的阿爾茨海默病小鼠模型中測試了CA,發現通過4到6個月的口服用藥,這兩種患病小鼠的記憶、抑鬱和焦慮問題均被改善,治療後的小鼠與健康的對照組小鼠無異或幾乎無異。
Cuervo補充道:“重要的是,這兩種模型中的動物都已顯示出了疾病的症狀,在給藥前,它們的神經元就已經被有毒蛋白質堵塞了。這意味著這種藥物甚至可以在疾病的後期幫助保持神經元功能。另一件讓我們感到興奮的發現是,該藥物還顯著減少了膠質增生(gliosesis)現象,即大腦神經元周圍的炎症和瘢痕。膠質增生與毒性蛋白質有關,目前已知它在神經退行性疾病的持續和惡化中起著重要的作用。”
研究顯示,即使長時間、每天服用CA,這種治療方式也似乎並不會損害到其他器官。該藥物是由生物化學和醫學教授、研究的共同領導者Evripidis Gavathiotis博士設計的。
據悉,Cuervo和Gavathiotis已與馬薩諸塞州波士頓(Boston,Mass)的Life Biosesciences公司合作,建立了Selphagy Therapeutics公司。該公司目前正在開發CA和相關化合物,用於治療阿爾茨海默病和其他神經退行性疾病。
翻譯:許楚楚
編輯:魏瀟
引進來源:Albert Einstein College of Medicine
本文來自:環球科學
關注【深圳科普】微信公眾號,在對話框:
回複【最新活動】,了解近期科普活動
回複【科普行】,了解最新深圳科普行活動
回複【研學營】,了解最新科普研學營
回複【科普課堂】,了解最新科普課堂
回複【科普書籍】,了解最新科普書籍
回複【團體定製】,了解最新團體定製活動
回複【科普基地】,了解深圳科普基地詳情
回複【觀鳥星空体育官网入口网站】,學習觀鳥相關科普星空体育官网入口网站
回複【博物學院】,了解更多博物學院活動詳情

圖片來源:Pixabay
美國阿爾伯特·愛因斯坦醫學院(Albert Einstein College of Medicine)的研究人員設計了一種實驗性藥物,它可以逆轉小鼠阿爾茨海默病(Alzheimer's disease)的主要症狀。該藥物的工作原理是恢複細胞的清潔機製,通過消化和循環的方式來清除不需要的蛋白質。研究已於2021年4月22日在線發表在《細胞》(Cell)雜誌上。
阿爾伯特·愛因斯坦醫學院衰老研究所(the Institute for Aging Research)的聯合主任、發育與分子生物學教授Ana Maria Cuervo是該研究的共同負責人,她對此介紹說:“以往,用小鼠做出的發現並不總能適用於人類,特別是在阿爾茨海默病的研究。但我們此次的研究發現,細胞清潔能力的衰退是阿爾茨海默病的成因之一,這種現象不僅體現在小鼠身上,還發生在人類患者身上。這一發現讓我們備受鼓舞,因為這表明該種藥物或許對人類也同樣有效。”20世紀90年代,Cuervo就發現了這類細胞清潔過程的存在,並將其稱之為“分子伴侶介導的自噬”(chaperone-mediated autophagy,CMA),已經發表了200餘篇有關於其在健康和疾病中的作用的論文。

Ana Maria Cuervo 圖片來源:Albert Einstein College of Medicine
隨著人們年齡的增長,CMA的效率逐漸降低,不必要的蛋白質積聚成有損細胞的不溶性塊狀物的風險也在逐漸增加。事實上,患者大腦中存在有毒蛋白質的聚合物,是阿爾茨海默病和其他所有神經退行性疾病的共有特征。《細胞》上發表的論文揭示了CMA和阿爾茨海默病的動態相互作用:神經元中CMA的缺乏會導致阿爾茨海默病,反之亦然。研究結果表明,加速CMA的藥物可能將為治療神經退行性疾病帶來希望。
建立CMA與阿爾茨海默病之間的聯係
在此項研究中,Cuervo的團隊首先研究了受損的CMA是否會導致阿爾茨海默病。為此,他們對一隻小鼠進行了基因改造,使其大腦內的興奮性神經元缺乏CMA。結果發現,僅一種類型的腦細胞缺失CMA就足以引起短期記憶喪失、行走障礙和其他一些在阿爾茨海默病的齧齒類動物模型中經常發現的問題。此外,在CMA缺失的情況下,蛋白質穩態(proteostasis)將被嚴重破壞,而這是細胞調節其所含蛋白質的能力。通常情況下,可溶性蛋白質會變為不可溶,具有凝結成有毒聚合物的風險。
Cuerve對該現象的逆向懷疑也是正確的:早期的阿爾茨海默症也同樣會損害CMA。她和同事們對一種相當於早期阿爾茨海默病的小鼠模型進行了研究,在這個模型中,小鼠的大腦神經元能產生tau蛋白的缺陷型拷貝。有證據表明,這種tau蛋白的異常拷貝會聚集在一起,形成神經原纖維纏結(neurofibrillary tangles),導致阿爾茨海默病產生。海馬(hippocampus)是對於記憶和學習而言至關重要的大腦區域,研究團隊重點研究了該區域神經元中的CMA活性,結果發現,與對照組的動物相比,患病小鼠神經元中的CMA活性顯著降低。
那處於早期的阿爾茨海默病的人類患者呢?它是否也阻礙了(人類細胞的)CMA?為了找到答案,研究人員對阿爾茨海默病患者死後的大腦神經元進行了單細胞RNA測序,並與一組來自健康個體的對照組數據進行了比較,希望了解CMA在患者腦組織中的活動水平。果然,處於阿爾茨海默病早期階段的患者,其CMA活性受到了一定程度的抑製;在阿爾茨海默症的晚期階段,這種抑製情況更為嚴重。
Cuervo表示:“當人們到了70或80歲時,CMA活動水平通常會比他們年輕時減少約30%。雖然大多數人的大腦可以彌補這種衰退,但如果此時再加上神經退行性疾病,這對大腦神經元的正常蛋白質組成可能是毀滅性的影響。我們的研究表明,CMA功能缺陷與阿爾茨海默病的病理過程協同作用,這將大大加速疾病的發展。”
一種“清潔”神經元的新藥
基於這一令人備受鼓舞的發現,Cuervo和團隊開發了一種新藥,這種藥物顯現出治療阿爾茨海默病的潛力。Cuervo介紹說:“我們知道CMA能夠消化有缺陷的tau蛋白和其他蛋白。但是阿爾茨海默病和其他神經退行性疾病中,大量的缺陷蛋白讓CMA不堪重負、並使其最終癱瘓。而我們的藥物能夠通過提高CMA關鍵成分的水平來重振CMA的效率。”
在CMA中,一種被稱為分子伴侶(chaperones)的蛋白質會與機體細胞中受損或有缺陷的蛋白質結合,並將它們當作“貨物”一般運輸至細胞的溶酶體(lysosomes)。作為一種內部充滿酶的膜結合型細胞器,溶酶體能起到消化和回收廢物的作用。然而,為了能成功地將這些“貨物”送入溶酶體,分子伴侶必須首先將它們“停靠”至稱為LAMP2A的蛋白質受體“船塢”上,而這種受體就長在溶酶體的膜上。溶酶體上的LAMP2A受體越多,CMA活性就可能越高。這款被稱為CA的新藥,就是通過增加LAMP2A受體的數量來發揮作用。

神經元內LAMP2A參與的細胞自噬。圖片來源:Courtesy of Albert Einstein College of Medicine
Cuervo解釋道:“人們一生中所產生的LAMP2A受體數量是相同的。但比起年齡的增加,這些受體的劣化速度更快。所以在老年人體內,將不需要的蛋白質輸送到溶酶體的可用受體往往更少。CA這款藥物能夠將LAMP2A的數量恢複至年輕水平,使CMA能夠有效擺脫tau蛋白和其他蛋白,這樣,它們就不會形成那些有毒的蛋白質團塊了。
同樣在4月,Cuervo博士的團隊在《自然-通訊》(Nature Communications)上報道稱,他們首次從阿爾茨海默病患者的大腦中分離出了溶酶體,並觀察到LAMP2受體數量的減少會導致人類CMA的喪失,就如同在動物模型中所發現的一樣。
研究人員在兩種不同的阿爾茨海默病小鼠模型中測試了CA,發現通過4到6個月的口服用藥,這兩種患病小鼠的記憶、抑鬱和焦慮問題均被改善,治療後的小鼠與健康的對照組小鼠無異或幾乎無異。
Cuervo補充道:“重要的是,這兩種模型中的動物都已顯示出了疾病的症狀,在給藥前,它們的神經元就已經被有毒蛋白質堵塞了。這意味著這種藥物甚至可以在疾病的後期幫助保持神經元功能。另一件讓我們感到興奮的發現是,該藥物還顯著減少了膠質增生(gliosesis)現象,即大腦神經元周圍的炎症和瘢痕。膠質增生與毒性蛋白質有關,目前已知它在神經退行性疾病的持續和惡化中起著重要的作用。”
研究顯示,即使長時間、每天服用CA,這種治療方式也似乎並不會損害到其他器官。該藥物是由生物化學和醫學教授、研究的共同領導者Evripidis Gavathiotis博士設計的。
據悉,Cuervo和Gavathiotis已與馬薩諸塞州波士頓(Boston,Mass)的Life Biosesciences公司合作,建立了Selphagy Therapeutics公司。該公司目前正在開發CA和相關化合物,用於治療阿爾茨海默病和其他神經退行性疾病。
翻譯:許楚楚
編輯:魏瀟
引進來源:Albert Einstein College of Medicine
本文來自:環球科學
關注【深圳科普】微信公眾號,在對話框:
回複【最新活動】,了解近期科普活動
回複【科普行】,了解最新深圳科普行活動
回複【研學營】,了解最新科普研學營
回複【科普課堂】,了解最新科普課堂
回複【科普書籍】,了解最新科普書籍
回複【團體定製】,了解最新團體定製活動
回複【科普基地】,了解深圳科普基地詳情
回複【觀鳥星空体育官网入口网站】,學習觀鳥相關科普星空体育官网入口网站
回複【博物學院】,了解更多博物學院活動詳情

做科普,我們是認真的!
掃描關注深i科普公眾號
加入科普活動群

- 參加最新科普活動
- 認識科普小朋友
- 成為科學小記者
下一篇:生活科普:毅力有那麽重要嗎?
 會員登錄
會員登錄














 深圳市龍華區玉翠社區高坳新村小廣場
深圳市龍華區玉翠社區高坳新村小廣場












