版權歸原作者所有,如有侵權,請聯係我們(men)
100多年前,卡爾梅特和介林在土豆片上的發現,讓人類戰勝了一種曾肆無忌憚奪取生命的可怕疾病;100多年後,卡介苗與(yu) 阿爾茨海默症的意外聯係是否會(hui) 打贏另外一場戰役,真實還是假象?科學終會(hui) 給出答案。
編譯 | 小葉
卡介苗,這一在中國幾乎盡人皆知、每個(ge) 新生兒(er) 都要接種的疫苗,正在成為(wei) 科學家的研究新寵。他們(men) 想用它來攻克另一百年難治之症——阿爾茨海默症,近幾年已經取得了多項進展。
澱粉樣蛋白的新認知
凡是知道阿爾茨海默症的人,對“澱粉樣蛋白假說”一定不陌生。盡管近年來該假說爭(zheng) 議不斷,它仍然是解釋阿爾茨海默症致病機理的主流理論,研究人員也以其為(wei) 靶點鑽研各種治療方法。該理論假定大腦中β-澱粉樣蛋白的漸進累積斑塊化,從(cong) 而觸發複雜的級聯反應:神經元細胞死亡,神經元突觸缺失,漸進性神經遞質愈發不足,所有這些效應最終導致癡呆的臨(lin) 床症狀。[1]
那麽(me) ,如果我們(men) 再往前溯源:導致β-澱粉樣蛋白斑塊化開始出現的確切原因是什麽(me) ?至今沒有答案。
2022年,一篇發表在《公共科學圖書(shu) 館:病原體(ti) 》(PLoS Pathogens)上的論文[2]提出了一條新的致病通路,即病原體(ti) 感染—免疫係統運作—β-澱粉樣蛋白累積—神經退行性疾病發生。具體(ti) 來說,當我們(men) 年輕時,自身防禦係統可以抵禦細菌、病毒或真菌進入大腦。然而,隨著年齡的增長,免疫細胞能力式微,微生物趁機進入神經組織中。而免疫係統生產(chan) β-澱粉樣蛋白以殺死入侵微生物,發揮短期的保護作用。如果大腦的免疫細胞,即小膠質細胞能正常工作,它們(men) 就能在病原體(ti) 危機解除之後,清除掉這些澱粉樣蛋白。但是,在許多阿爾茨海默症患者病例中,小膠質細胞似乎出現了功能障礙,無法及時清理,澱粉樣蛋白質由此不斷沉積、斑塊化,反過來開始損傷(shang) 神經元。實際上,上世紀90年代發表的相關(guan) 屍檢報告[3]就發現,阿爾茨海默症逝者大腦中寄生著常見的微生物,例如引發唇皰疹的1型單純皰疹病毒,這些微生物通常被困於(yu) 澱粉樣蛋白中。
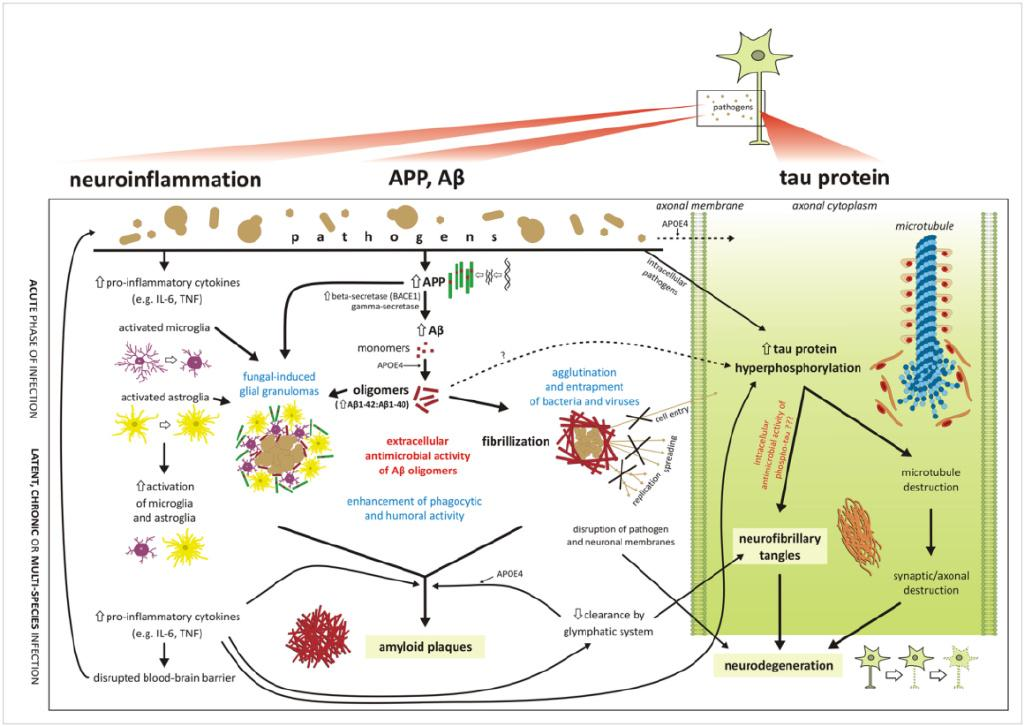
圖1:圖片展示了病原體(ti) 感染中樞神經係統後,激活免疫反應,其中β-澱粉樣蛋白累積便是消除病原體(ti) 的手段之一,但隨後也會(hui) 形成澱粉樣蛋白沉積斑塊。來源:
10.1371/journal.ppat.1010929
其實學界已有研究報告β-澱粉樣蛋白質另一不為(wei) 人知的特性:可抵抗微生物。2018年發表在《阿爾茨海默症期刊》(Journal of Alzheimer’s Disease)上的綜述文章文[4]提供諸多研究證據,表明在人類和動物模型內(nei) ,大腦感染後進一步刺激了β-澱粉樣前體(ti) 蛋白的加工,包括降解切割後由40-和42-氨基酸殘基組成的蛋白的生成,這兩(liang) 種蛋白質也是阿爾茨海默症患者腦內(nei) β-澱粉樣蛋白的主要存在形式,它們(men) 容易纖維化聚集起來,形成不同大小的可溶性聚集體(ti) ,β-澱粉樣蛋白寡聚體(ti) 便是其中一種[5],科學家通過在體(ti) 和體(ti) 外實驗表明這些寡聚體(ti) 具有強效的廣譜抗菌特性,可捕獲病原體(ti) ,破壞其細胞壁,持續抵抗細菌和病毒的感染。而清除β-澱粉樣蛋白的阿爾茨海默症的臨(lin) 床試驗,則觀測到患者隨後感染程度有所增加。
同年,另一篇研究[6]則通過小鼠模型和人類神經元細胞培養(yang) 感染模型,揭示了β-澱粉樣蛋白寡聚體(ti) 可結合皰疹病毒表麵糖蛋白,一方麵加速β-澱粉樣蛋白沉積,另一方麵對嗜神經性單純皰疹病毒 1 (HSV1) 和人類皰疹病毒 6A 和 B 展開捕獲。再次支持β-澱粉樣蛋白可能在中樞神經係統先天免疫過程發揮保護性作用的說法。
由此可見,β-澱粉樣蛋白的短暫活動有助於(yu) 大腦消滅入侵微生物,但隨後卻因免疫功能障礙從(cong) “得力助手”成為(wei) 可能的“致病殺手”。事實上,靶向β-澱粉樣蛋白一直是多年來學界設計阿爾茨海默症治療藥物的策略之一,經過幾十年的研究,美國食品藥品監督管理局僅(jin) 批準了兩(liang) 款治療早期阿爾茨海默症的單克隆抗體(ti) 藥物:ADUHELM[7]和Leqembi[8],它們(men) 能選擇性結合患者大腦中β-澱粉樣蛋白沉積斑塊,將其中和並消除,能緩解部分患者的疾病進展,但整體(ti) 生活質量的改善往往有限,還有一定的不良反應[9]。
而對β-澱粉樣蛋白特性的新認識提供了另一對抗思路:如果能增強免疫係統的整體(ti) 功能而不隻為(wei) 消除β-澱粉樣蛋白沉積,或許就能讓免疫細胞及時清除沉積的斑塊,防止進一步病變的發生。
百年老藥展現新用途
有時候,科學發現往往出現在最讓人意想不到的地方。
讓我們(men) 先回到20世紀初的法國,醫生阿爾貝·卡爾梅特(Albert Calmette)和獸(shou) 醫卡米爾·介林(Camille Guérin)合力尋找牛結核病傳(chuan) 播的途徑。為(wei) 實現這個(ge) 目的,他們(men) 首先需要培養(yang) 出牛結核病菌,倆(lia) 人發現將切片的土豆和牛膽、甘油一起煮熟,能“熬製”出完美的病菌培養(yang) 基。不過在培養(yang) 過程中,他們(men) 驚訝地發現隨著每一代細菌的生長,它們(men) 的毒力會(hui) 越來越弱,一代不如一代。隨後,動物即便感染了多代培養(yang) 出來的細菌,它們(men) 非但不再生病,而且還不會(hui) 再受到野生結核病菌的感染。到了1921年,兩(liang) 位醫生在首個(ge) 人類患者身上進行測試,受試對象是一名嬰兒(er) ,他的母親(qin) 剛死於(yu) 肺結核沒多久,結果奏效了。於(yu) 是,在日後拯救下數百萬(wan) 生命的卡爾梅特-介林疫苗(亦稱為(wei) 卡介苗)由此誕生,並得到了廣泛接種。
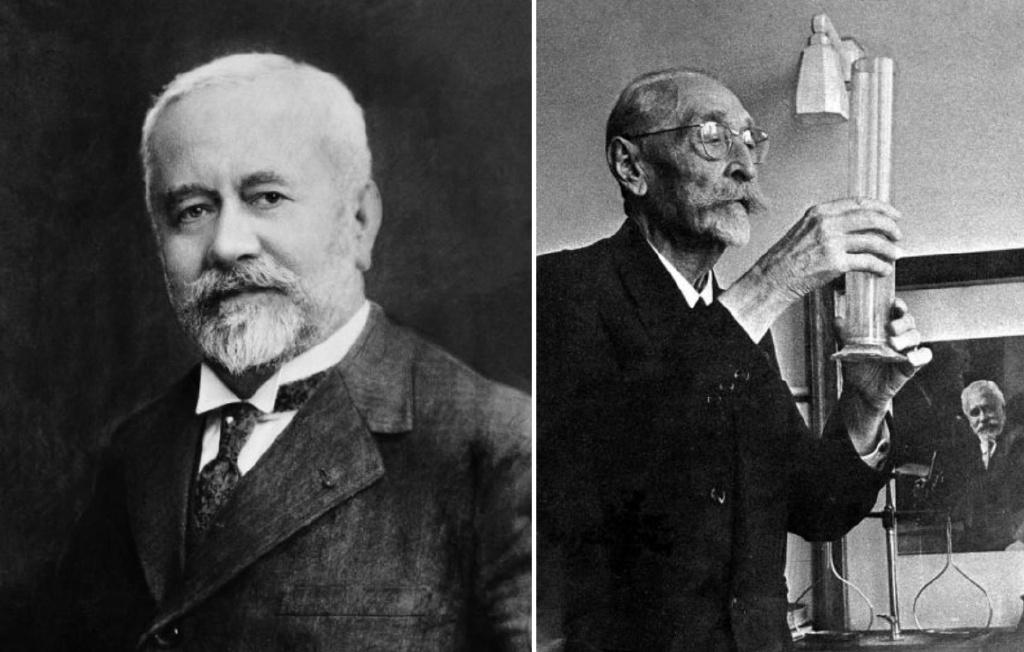
發明卡介苗的兩(liang) 位醫生,左圖為(wei) 醫生阿爾貝·卡爾梅特(Albert Calmette),右圖為(wei) 獸(shou) 醫卡米爾·介林(Camille Guérin)
然而,卡爾梅特和介林生前可能從(cong) 未想到,自己的研究可能啟發一個(ge) 多世紀後的科學家,將卡介苗用於(yu) 研究另一種截然不同的疾病,而且還得出了令人意想不到的結論:卡介苗可能保護人們(men) 大腦,以免發展出阿爾茨海默症。
這個(ge) 說法聽上去好像很離譜,但數十年來學界確實展開研究,表明卡介苗的保護範圍出乎意料的廣泛,遠超其最初研發目的。例如,發表在《疫苗》(Vaccines)期刊上的一篇薈萃分析研究文[10]揭示卡介苗可降低呼吸道感染風險。而另一篇雙盲隨機臨(lin) 床實驗[11]則表明對於(yu) 呼吸道感染風險,接種卡介苗可提供強勁的保護效力。
除了呼吸道感染,卡介苗還作為(wei) 非肌層浸潤性膀胱癌的標準治療手段:將減毒細菌遞送到器官中,能激活免疫係統去消滅腫瘤,由此可降低腫瘤複發的風險,降低癌症進一步發展成更具侵襲性疾病的可能性。[12]
甚至在新冠大流行期間,一些研究認為(wei) 卡介苗可能對新冠病毒感染有保護作用。例如美國弗吉尼亞(ya) 理工大學、國家過敏與(yu) 傳(chuan) 染病研究所等機構研究人員,就於(yu) 2020年7月在《美國國家科學院院刊》(PNAS)上發表報告稱[13],他們(men) 回顧了卡介苗預防新冠病毒感染的潛在生物學證據,在排除潛在幹擾因素後,發現在國情相似的各歐洲國家,一個(ge) 國家的卡介苗接種率與(yu) 新冠病亡率之間存在顯著相關(guan) 性。卡介苗接種率每提高約10%,新冠病亡率就會(hui) 降低10.4%。
具體(ti) 到卡介苗治療阿爾茨海默症,已有動物模型研究提供了一些初步證據。2017年,中國中山大學中山醫學院團隊發表論文[14],通過阿爾茨海默症小鼠模型實驗發現,接種卡介苗的小鼠大腦中發揮炎症消退作用的單核細胞募集得到了增強,聚集到大腦中斑塊病變區域;與(yu) 此同時,還生成了更多可增強免疫功能的循環幹擾素-γ,抗炎細胞因子水平得到了上調,最終模型小鼠腦部炎症得到緩解。
卡介苗之所以能在上述各研究中發揮免疫增強效果,得益於(yu) “免疫係統訓練”這一過程。當個(ge) 體(ti) 接種卡介苗之後,與(yu) 細胞因子生成相關(guan) 的基因表達發生變化。細胞因子是一種能夠激活我們(men) 身體(ti) 內(nei) 其他防禦機製,包括白細胞在內(nei) 的小分子,從(cong) 而讓身體(ti) 更有效地應對威脅,包括外來入侵的病毒或細菌,或者生長不可控的細胞突變等。
如此一來,卡介苗的“免疫係統訓練”便與(yu) 前文提出的通過增強免疫係統來預防阿爾茨海默症的設想聯係到了一起:通過訓練,身體(ti) 的防禦能力得到了增強,將病原體(ti) 阻擋在進入大腦之前。此外,增強的免疫係統還能及時有效地清除大腦中的β-澱粉樣蛋白,且不傷(shang) 害健康的神經組織。
好消息不斷,但仍需保持謹慎
既然在小鼠模型實驗中,卡介苗接種產(chan) 生了積極效果,那麽(me) 對人類來說是否也同樣奏效呢?為(wei) 回答這個(ge) 問題,全球多個(ge) 研究團隊展開了探索。
來源:pixabay
耶路撒冷希伯來大學哈薩德醫學中心(Hadassah Hebrew University Medical Center)的Ofer Gofrit團隊收集了1371名平均年齡為(wei) 68.1歲的膀胱癌患者相關(guan) 數據,他們(men) 或接受過,或未接受過卡介苗治療。在之後的隨訪期間,發現接受過卡介苗治療的患者罹患阿爾茨海默症的風險要比未接受過卡介苗治療的患者低4倍以上[15]。該結果於(yu) 2019年發表在《公共科學圖書(shu) 館:病原體(ti) 》(PLOS ONE)期刊上,之後其他研究團隊成功複現了這一結果。
2023年,美國波士頓麻省總醫院(Massachusetts General Hospital)的Marc S. Weinberg團隊在《JAMA開放網絡》 (JAMA Network Open)上發表了隊列研究結果[16],他們(men) 調查了馬薩諸塞州約6500名非肌層浸潤性膀胱癌老年患者,發現卡介苗治療與(yu) 更低的阿爾茨海默症以及相關(guan) 癡呆症風險相關(guan) 聯。
不過,不同研究闡釋出卡介苗降低阿爾茨海默症疾病風險的不同程度。2023年8月的一項薈萃分析同樣以卡介苗治療對膀胱癌患者癡呆症風險的影響為(wei) 課題[17],搜尋了直到2023年5月20日的六大相關(guan) 數據集,評估了4043份記錄,最終分析了5篇包括45407名患者的研究論文,結果表明卡介苗與(yu) 膀胱癌患者癡呆症發病率之間存在顯著相關(guan) 性,而接受卡介苗治療可平均降低45%的癡呆症發病率。
45%這個(ge) 數字,讓人意外又欣喜。然而,這隻是一項薈萃研究,仍需深入研究繼續證實。如果情況確實如此,那將對預防阿爾茨海默症產(chan) 生巨大影響。耶路撒冷希伯來大學的Charles Greenblatt教授對此評價(jia) 說:“僅(jin) 僅(jin) 將阿爾茨海默症的發展延後幾年,都將極大減輕人們(men) 的痛苦,節省大量金錢。”[18]
盡管好消息不斷,但非常有必要始終保持謹慎。首先,現有的論文報告基本上都以膀胱癌患者為(wei) 研究對象,對一般人群的數據少之又少。一條明顯的研究策略是比較童年時期接種卡介苗與(yu) 未接種卡介苗的人,但缺點也很突出:卡介苗的效果可能會(hui) 隨著幾十年時間的流逝而變得微乎其微,甚至遠早於(yu) 大多數人患上阿爾茨海默症的危險期。
其次,這些研究都沒有給出因果關(guan) 係證明,均為(wei) 相關(guan) 性證明。“在流行病學研究中,可能潛伏著各種混淆因素,研究人員可能沒有充分考慮這些潛伏因素。”賓夕法尼亞(ya) 州德雷克塞爾大學醫學院(Drexel University College of Medicine)的Jeffrey Lapides說,盡管他認同卡介苗對癡呆症的影響具有合理性,但仍需更多研究來證明。確定性的證據要求展開隨機對照試驗,分配患者或接受治療,或服用安慰劑。然而,癡呆症的發展是一個(ge) 相當緩慢且漫長的過程,可能需要數年甚至更久的時間來收集更多數據,以證明卡介苗或其他疫苗能夠提供理想的保護效力,預防阿爾茨海默症。
威斯康星大學麥迪遜分校(University of Wisconsin-Madison)的Coad Thomas Dow團隊展開了一項試點研究,並於(yu) 2022年將成果發表在Microorganisms期刊上[19],團隊招募了49名受試者,發現卡介苗接種可有效降低血漿澱粉蛋白質水平,特別是在攜帶與(yu) 更高阿爾茨海默症風險相關(guan) 基因的受試者中。另外,更年輕受試者、風險級別更高的受試者、未潛伏性感染巨細胞病毒的受試者,以及淋巴細胞免疫風險情況良好的受試者都表現出統計學意義(yi) 上顯著的有利變化。盡管該研究樣本量很小,但增強了繼續鑽研通過免疫訓練來預防阿爾茨海默症這一策略的信心。
受到卡介苗相關(guan) 新研究的啟發,有些科學家也盯上了其他疫苗。雖然卡介苗被認為(wei) 可提供最強效的免疫訓練,因為(wei) 它包含減毒的活體(ti) 細菌,但其他疫苗也有刺激身體(ti) 免疫係統的作用,例如流感疫苗。已有隊列分析研究表明[20],在控製了混雜因素後,與(yu) 未接種過流感疫苗的受試者相比,接種過流感疫苗、平均年齡為(wei) 75.5歲的受試者罹患癡呆症的可能性顯著更低。
而意大利巴勒莫大學(UNIPA)的Nicola Veronese團隊分析了9項研究結論[21],其中許多控製了生活方式因素,包括收入、教育程度、吸煙、飲酒和高血壓,結果發現,流感疫苗與(yu) 癡呆症風險降低29%之間相關(guan) 聯,而且疫苗接種劑量與(yu) 癡呆症發病率之間也存在關(guan) 聯性。
致力於(yu) 通過疫苗預防阿爾茨海默症的醫學專(zhuan) 家們(men) 持有樂(le) 觀態度,Weinberg活躍在研究前沿,他與(yu) Steven Arnold博士和Denise Faustman博士合作研究,收集已接種過或未接種過疫苗的受試者中樞神經係統周圍的腦脊液樣本,他們(men) 的目的是檢查疫苗觸發的免疫訓練效果是否能達到大腦。Weinberg說:“卡介苗接種後,這些免疫細胞對病原體(ti) 的反應更加強烈了。”
根據世界衛生組織於(yu) 2023年公布的統計數據,目前全世界有超過5500萬(wan) 人患有癡呆症,其中阿爾茨海默症是最常見的形式,可能占患病人數的60%至70%。[22]如果疫苗能夠為(wei) 治療阿爾茨海默症發揮作用,那真是善莫大焉。
100多年前,卡爾梅特和介林在土豆片上的發現,讓人類戰勝了一種曾肆無忌憚奪取生命的可怕疾病;100多年後,卡介苗與(yu) 阿爾茨海默症的意外聯係是否會(hui) 打贏另外一場戰役,真實還是假象,科學終會(hui) 給出答案。
參考文獻
[1] https://www.msdmanuals.cn/professional/neurologic-disorders/delirium-and-dementia/alzheimer-disease
[2] https://journals.plos.org/plospathogens/article?id=10.1371/journal.ppat.1010929
[3] https://onlinelibrary.wiley.com/doi/10.1002/jmv.1890330403
[4] https://content.iosespress.com/articles/journal-of-alzheimers-disease/jad171133
[5] https://www.alzcn.com/CN/10.3969/j.issn.2096-5516.2023.01.001
[6] https://www.sciencedirect.com/science/article/pii/S0896627318305269
[7] https://www.fda.gov/drugs/drug-approvals-and-databases/drug-trials-snapshots-aduhelm
[8] https://www.fda.gov/news-events/press-announcements/fda-converts-novel-alzheimers-disease-treatment-traditional-approval
[9] https://www.nejm.org/doi/full/10.1056/NEJMoa2212948
[10] https://www.mdpi.com/2076-393X/11/1/121
[11] https://www.cell.com/cell/fulltext/S0092-8674(20)31139-9?_returnURL=https%3A%2F%2Flinkinghub.elsevier.com%2Fretrieve%2Fpii%2FS0092867420311399%3Fshowall%3Dtrue
[12] https://www.mdpi.com/2072-6694/14/13/3073
[13] https://www.pnas.org/doi/full/10.1073/pnas.2008410117
[14] https://www.sciencedirect.com/science/article/abs/pii/S096999611730030X?via%3Dihub
[15] https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0224433
[16] https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2805030
[17] https://www.frontiersin.org/articles/10.3389/fnagi.2023.1243588/full
[18] https://www.theguardian.com/society/2024/feb/25/is-the-100-year-old-tb-vaccine-a-new-secret-weapon-against-alzheimers-dementia-bcg
[19] https://www.mdpi.com/2076-2607/10/2/424
[20] https://www.sciencedirect.com/science/article/abs/pii/S0264410X21010793
[21] https://www.sciencedirect.com/science/article/abs/pii/S1568163721002816
[22] https://www.who.int/zh/news-room/fact-sheets/detail/dementia
[23] https://www.theguardian.com/society/2024/feb/25/is-the-100-year-old-tb-vaccine-a-new-secret-weapon-against-alzheimers-dementia-bcg
歡迎掃碼關(guan) 注深i科普!
我們(men) 將定期推出
公益、免費、優(you) 惠的科普活動和科普好物!



- 參加最新科普活動
- 認識科普小朋友
- 成為科學小記者
 會員登錄
會員登錄














 深圳市華強北街道 華新地鐵站A1出口24小時科學銀行
深圳市華強北街道 華新地鐵站A1出口24小時科學銀行












